課題3「予測医療に向けた階層統合シミュレーション」(代表:東京大学・高木 周教授)は、昨年春に終了したグランドチャレンジプログラムで個別に開発が進められてきた生体シミュレータ(血栓症、心臓、筋骨格、脳神経系など)を統合し、心筋梗塞をはじめさまざまな疾患における複雑なプロセスを再現し、病態の予測や治療の支援に貢献することをめざしている。新たに開発される統合シミュレータのモデル開発では、「京」の高い計算能力を有効に活用し、分子レベルから生体レベルのすべてを数値表現するマルチスケール、力学的現象、生化学反応、電気的現象といったいろいろな現象を扱うマルチフィジックスを同時に実現することが求められている。今回は、多くの課題と向き合いながら、課題3の研究開発に取り組む3名の研究者に話を聞いた。


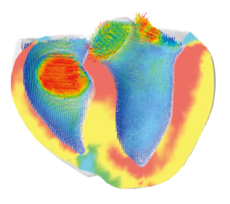
心臓シミュレータ
(UT-Heart)で再現された心室
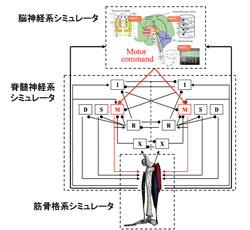
全身筋骨格-神経系統合シミュレーションの概念図
階層統合によるモデル構築が必要
━
みなさんは具体的にどのような研究に取り組んでいるのですか。
清水
私と山村さんは、例えばパーキンソン病のような神経疾患による運動機能障害の解明をめざして、生体内で起きているミクロからマクロまでの活動を再現する、人間の全身筋骨格-神経系統合シミュレーションモデルの開発を進めています。脳で運動指令がつくられて、脊髄などの信号伝達経路でさまざまに修飾され、最終的に筋肉が収縮したり、関節が動く。そうした一連の過程をコンピュータ上でシミュレーションできるようにして、病気の原因究明や治療に貢献するのが、私たちの研究開発の目的です。そのなかで、私が主に担当しているのは、脊髄の神経ネットワークモデルの構築です。
山村
私は、脊髄からの指令をたとえば四肢の筋肉で受け取り、筋肉が収縮して関節運動が行われる、そうした筋骨格系の運動シミュレータを開発しています。脳については別のグループが担当していて、今後、脳・脊髄・筋骨格系をひとつに統合していく予定です。
鷲尾
私たちのグループは、生きた心臓そのものを「京」で再現する心臓シミュレータ(UT-Heart)の開発を進めています。そのなかで、今は心臓の拍動のモデル化に取り組んでいます。基本的には、個々の分子の動きをもとに、物理法則に従った方程式を解きながら、拍動をコンピュータ上で再現しようというわけです。とはいえ、分子が単独で動いているのではなく、他の分子やまわりの筋肉などの影響を受けるため、平均的な動きを記述する方程式をつくることはとても難しい。さらに分子に働く力から、よりマクロな連続体にかかる力を計算して心筋の動きを再現するだけでなく、心臓から拍出される血液という流体と心室壁との相互作用を解かなければなりません。その血液も心臓単独で計算できるわけではなく、体全体の血液の流れを再現する必要があります。そのためには、「京」のような大きな計算資源を活用して、分子から体循環まで一貫して扱わなければ、現象がうまく再現できないのです。
山村
骨格筋の場合も、基本的には心筋とほぼ同じです。私たちも今ちょうど、鷲尾さんが取り組んでいるように、筋肉の収縮や関節運動を分子レベルから立ち上げるモデルを構築しているところです。
清水
神経系では、細胞の表面にある穴を閉じたり開いたりして、内外にミネラル分を移動させることで電気信号をやり取りしています。そのため、信号伝達のシミュレーションでも、分子よりやや大きいですが、細胞レベルより分子に近いスケールを含むモデル構築に取り組んでいます。脳神経系に比べれば、関節をひとつ動かす程度のシミュレーションでは、それほど大きな計算資源は必要ありませんが、将来的に「歩いたり、走ったり」といった全身を使う動きを視野に入れた場合は、脊髄神経系だけでもかなり大きな計算資源が必要になってきます。
モデル化のための基礎的な情報取得が難しい
━
シミュレータ構築を進める上で、最も苦労しているのはどのような点ですか。
清水
生命科学分野に携わる前は、主に流体のシミュレーションをやっていたのですが、例えば工学的なシミュレーションの場合は、基本になる詳細な設計図があり、電気抵抗や熱伝導率を調べるなど、モデル化に必要な材料試験も比較的簡単にできます。しかし対象が人体となると、すぐに解剖して測るわけにもいきませんから、基礎的な情報がなかなか得られない難しさがあります。
山村
私も生体を扱う前は、主に金属薄板の成形シミュレーションなどをやっていましたから、人体の基礎的なデータを手に入れることの難しさや苦労を実感しています。特に私たちは、“生きている人体”で測りたいわけです。なるべく針を刺したりせず、非侵襲で測定できればいいのですが、それもなかなか難しい。さらに、個人差も非常に大きい。骨格筋の形状などは、MRIのデータなどを利用していますが、例えば骨につながって筋収縮の力を伝える腱膜などは、薄くてうまく写りません。測定できないものは、解剖学的な文献などに頼るしかないのが実情です。
清水
神経系は、おそらく筋骨格以上に測定が困難だと思います。
鷲尾
心臓も同様です。例えば心臓の形については、CTスキャンやMRIのデータがありますが、心臓は絶えず動いていますので、生きている人間の自然な形状は、正確には分からないし、個人差もあります。また心筋は非常に複雑で、筋線維がねじれるように走っており、15%ほど縮むだけで約60%の血液を拍出できるという非常に巧妙な構造を持っています。そうした詳しい構造も、現在の計測技術では解剖するか、心臓を止めない限り調べることができません。私たちにできるのは、可能な限り多くのデータや実験結果を集めて、特徴的な現象を余すところなく再現できるモデルをつくり上げるということです。
社会に貢献できるシミュレータの開発をめざす
鷲尾
幸いなことに、「京」が使えるようになって心臓シミュレータの信頼性が向上したことから、分子生物学で実験を中心に取り組んでおられる研究者や心臓外科の医師の方々も、シミュレーションに高い関心を持ってくださるようになり、実験を引き受けていただいたり、データを提供していただける協力関係が広がりつつあります。また、生まれながらに心臓に欠陥がある患者さんの手術方法を決める際に、シミュレーションが活用できないかという話も出ています。一方では、心臓シミュレータを利用して肥大型心筋症という病気の発症メカニズムを明らかにするチャレンジも始まっています。臨床医学と基礎医学の両面で心臓シミュレータが役に立てると同時に、そこから得られる成果によって、さらにシミュレーションモデルを高度なものにしていけるのではないかと考えています。
山村
医療現場や分子生物学の基礎研究者とシミュレーション科学が協力しながら、お互いに高め合ってくというのは、素晴らしいことですね。全身筋骨格-神経系統合シミュレーションの場合は、まだモデル開発の段階ですが、もう少し進めば、医療現場や基礎研究者にも興味を持っていただけると思っています。
清水
例えば、パーキンソン病はその発症メカニズムさえもよく分かっていませんが、シミュレーションによって明らかにされ、治療方針を決める際に役立つようになれば、状況は大きく変わるはずです。シミュレーション科学が医療にとっても、基礎研究にとっても役立つものだということを実証していくことは、私たちの大事な役割のひとつですね。
鷲尾
さらに、医療現場の医師と分子生物学の研究者は、実際はあまりつながっていませんが、階層統合シミュレーションはその橋渡しができるかもしれません。そのためにも、シミュレータの信頼性を高めていくことが重要です。
山村
社会に貢献できる、確かな成果を生み出していかなければいけないということですね。
鷲尾
シミュレータは、単に論文を書くための道具ではなく、社会に役立つものだと認めてもらえるものに仕上げていくことが、このプロジェクトに参加する私たちのゴールなのだと思います。
